公共卫生学术热点追踪
NEJM:中和抗体滴度超过康复患者,Moderna新冠疫苗1期临床详细结果发表
Moderna公司开发的针对新冠病毒的mRNA疫苗(mRNA-1273)在1期临床试验的中期结果,在《新英格兰医学杂志》发表。试验结果表明,100%受试者中观察到了针对新冠病毒的中和抗体,在100 μg剂量水平,受试者的中和抗体几何平均滴度高于康复患者血清中观察到的几何平均滴度。这一剂量被选为在即将进行的3期临床试验中使用的疫苗剂量。

截图来源:New England Journal of Medicine
在这项试验中,45例年龄为18-55岁的健康成人受试者间隔28天,接受了两剂不同剂量水平(25、100、250 μg)的mRNA-1273接种。截至接种后第57天的结果显示,mRNA-1273诱导了针对新冠病毒的快速和强烈的免疫应答。这项研究由美国国立卫生研究院(NIH)下属的国家过敏和传染病研究所(NIAID)领导进行。
免疫原性反应
mRNA-1273诱导所有受试者在首次接种后第15天产生能够与全长新冠病毒刺突蛋白结合的抗体。在接种两次疫苗后的第57天,几何平均滴度超过了从确诊为COVID-19的38例患者中获得的恢复期血清的几何平均滴度。 研究人员用两种不同的检测评估了中和抗体活性,一种是活新冠病毒蚀斑减少中和试验(PRNT),另一种是假病毒中和试验(PsVNA)。接种疫苗前,没有受试者检测到PRNT或PsVNA反应。 两次接种后,mRNA-1273引起了高水平的中和抗体免疫反应。第43天时,在所有评价的受试者中观察到抗新冠病毒的中和抗体活性(PRNT)。在100 μg剂量下,几何平均滴度水平是参比康复患者血清(n=3)中观察到水平的4.1倍。 第二次接种后,在所有剂量队列的受试者中检测到PsVNA中和抗体滴度。100 μg剂量下第57天的几何平均滴度比恢复期血清(n=38)中观察到的滴度高2.1倍。
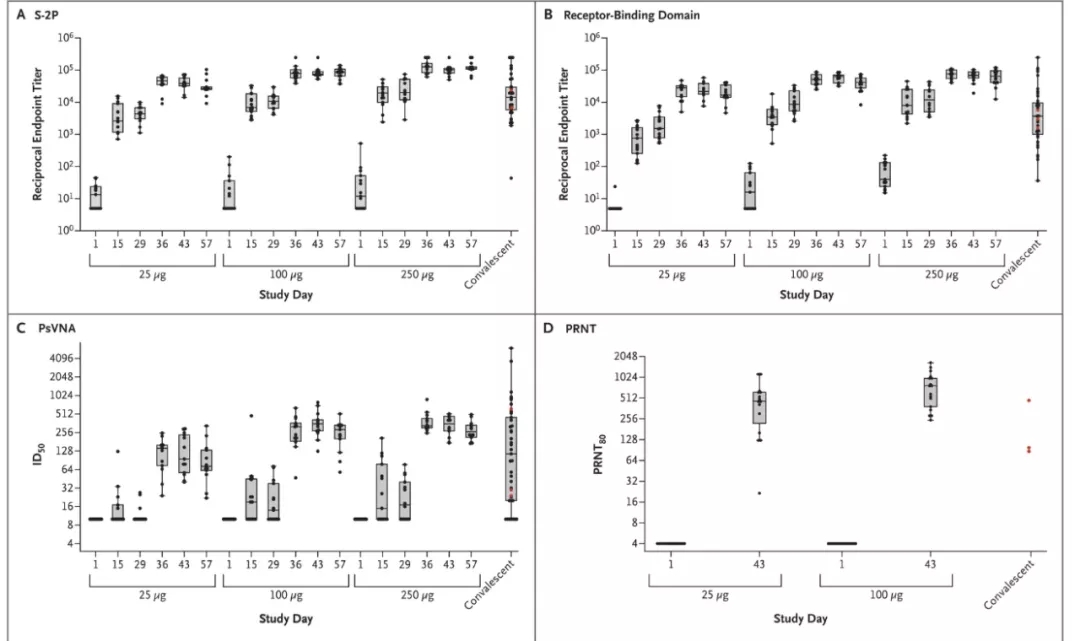
▲mRNA-1273引发的免疫反应数据
研究人员还在25 μg和100 μg剂量水平下评估了T细胞的免疫应答。第二次接种后,mRNA-1273引起Th1偏倚的CD4阳性T细胞应答,而Th2偏倚的CD4阳性T细胞应答无显著升高。
安全性特征
在安全性方面,mRNA-1273的安全和耐受性良好,直至第57天未报告严重不良事件。不良事件(AE)严重程度通常为轻度至中度,且为一次性事件。第二次接种后,25 μg组13例受试者中有7例(54%)、100 μg组所有15例受试者和250 μg组所有14例受试者中都有发生全身性不良事件。100 μg剂量第二次接种后,最常报告的全身不良事件为疲乏(80%)、寒战(80%)、头痛(60%)和肌痛(53%),严重程度为轻度或中度。100 μg剂量组最常见的局部不良事件是注射部位疼痛(100%),严重程度为轻度或中度。
“这些积极的1期数据令人鼓舞,代表着我们的候选疫苗mRNA-1273临床开发向前迈出了重要的一步。Moderna团队本月将继续专注于启动我们的3期研究,如果成功的话,将提交生物制品许可申请,”Moderna首席执行官Stéphane Bancel先生说:“我们致力于尽可能快速和安全地推进mRNA-1273的临床开发,同时投资扩大生产规模,以便帮助解决这一全球卫生紧急情况。”公司预计3期临床试验将在7月27日展开,使用的接种剂量为100 μg。预计这一试验将招募3万名参与者。
Moderna
(来源:药明康德)
参考文献:
[1] Moderna Announces Publication in The New England Journal of Medicine of Interim Results From Phase 1 Study of Its mRNA Vaccine Against COVID-19 (mRNA-1273). Retrieved July 14, 2020, from https://www.businesswire.com/news/home/20200714006042/en
[2] Jackson et al., (2020). An mRNA Vaccine against SARS-CoV-2 — Preliminary Report. NEJM, DOI: 10.1056/NEJMoa2022483
链接:https://mp.weixin.qq.com/s/vfOloIo8EJJSbYAvpAKM9w
