公共卫生学术热点追踪
朱轩 /陈福和/袁国勇团队最新研究进展:新冠病毒变异株跨越宿主屏障感染大鼠和小鼠
新型冠状病毒(SARS-CoV-2)的受体血管紧张素转化酶2(ACE2)在小鼠中表达的氨基酸序列与人不同,其刺突蛋白与小鼠源ACE2(mACE2)以及大鼠源(rACE2)的结合能力低,导致SARS-CoV-2难以感染鼠科动物。但病毒基因组在传播的过程中不断进化,尤其在刺突蛋白的受体结合区域(receptor binding domain)累积了不同的突变,从而拓宽病毒的易感宿主。
2021年10月21 日,香港大学朱轩/陈福和/袁国勇研究团队在EBioMedicine发表题为 Emerging SARS-CoV-2 variants expand species tropism to murines 文章(帅惠萍博士、陈福和博士和袁梓泰为共同第一作者,朱轩博士、陈福和博士和袁国勇院士为共同通讯作者),揭示在病毒传播过程中自然出现的、正在世界范围内广泛流行的多个引起关注变异株(VOC)均显著提高了病毒刺突蛋白与mACE2和rACE2结合能力,从而增强了这些变异株对过表达mACE2和rACE2受体的细胞的感染力。研究团队进一步利用B.1.1.7(Alpha系),B.1.351(Beta系),P.3(Theta系)和B.1.617.2(Delta)四种变异病毒株感染小鼠和大鼠,结果证实携带N501Y突变的变异病毒能够感染小鼠和大鼠的上呼吸道以及肺上皮细胞并进行高效的复制和繁殖。

团队首先利用假病毒系统研究五种来自不同变异株系的刺突蛋白分别对小鼠/大鼠/人ACE2受体的感染力,发现Alpha-, Beta-, Gamma-系的假病毒对小鼠和大鼠ACE2受体的感染力显著提高。通过分析这些变异株的刺突蛋白受体结合区域,发现它们的共同突变N501Y显著提高了假病毒对过表达小鼠和大鼠ACE2细胞的入侵力。进一步的真病毒实验证实,B.1.1.7, B.1.351和P.3除了能够利用人源ACE2之外,还能够利用mACE2和rACE2进行病毒感染,与之对照,德尔塔株则只能利用人源ACE2。
为了验证细胞水平的发现,团队利用C57B6品系的小鼠进行动物感染实验。结果显示,被携带N501Y突变的变异株感染的小鼠,上呼吸道以及肺中的病毒载量显著高于非变异的原始毒株感染的小鼠的病毒载量。并且通过检测冠状病毒复制过程的中间产物subgenomic RNA,证实变异株在非转基因小鼠的呼吸道中能够进行高效复制并且产生高滴度的子代病毒。
另外,在大鼠感染实验中,也证实携带N501Y突变的变异病毒能够有效地感染大鼠,并在大鼠的上呼吸道以及肺中引起明显的病理损伤。
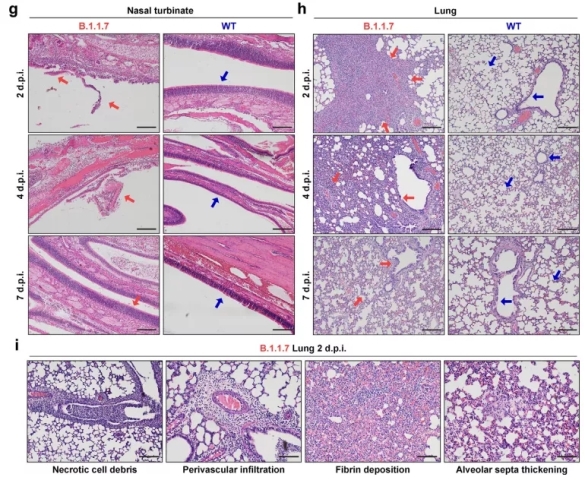
图1. N501Y突变新冠毒株所造成的大鼠上呼吸道及肺部损伤
在发现部分变异病毒株能够感染非转基因小鼠之前,研究人员尝试通过在小鼠体内连续传代产生突变病毒或者人源化ACE2转基因小鼠的方法来建立SARS-CoV-2的小鼠感染模型。其中,K18-hACE2转基因小鼠是将hACE2插入到上皮细胞启动子K18下游而构建成功的小鼠感染模型,并被广泛应用为SARS-CoV-2感染动物模型,但由于外源性的基因插入改变了ACE2在小鼠组织中的分布,从而可能改变病毒的组织嗜性,因而K18-hACE2转基因不一定能够如实反映SARS-CoV-2体内感染的特性。
团队的研究结果提示,SARS-CoV-2在自然进化的过程中获得了适应性突变,使其跨越了宿主屏障,能够感染非转基因的小鼠和大鼠。由于鼠类动物的数目庞大并且与人类生活关系密切,因此变异株所带来的公共卫生挑战不能忽视。另外,本研究发现也为建立SARS-CoV-2的小鼠感染模型打开新思路。
(来源:生命科学前沿)
原文出处:Huiping Shuai, Jasper Fuk-Woo Chan, Terrence Tsz-Tai Yuen, et al. Emerging SARS-CoV-2 variants expand species tropism to murines[J]. October 21, 2021.
链接:https://www.thelancet.com/journals/ebiom/article/PIIS2352-3964(21)00436-9/fulltext
