公共卫生学术热点追踪
Nat Cell Biol | 田瑞琳等发现宿主细胞控制新冠病毒感染新靶点
新冠病毒肆虐全球,开发有效的抗病毒手段仍是当务之急。新冠病毒的感染离不开病毒和宿主两个部分。新冠病毒通过刺突蛋白(Spike protein)结合宿主细胞表面的受体(主要为ACE2)感染宿主细胞。因此,可以从病毒和宿主细胞两个角度出发来开发阻止病毒感染的方法。目前全球的新冠防治策略,包括疫苗、中和抗体以及小分子药物大都是从靶向病毒的角度出发,而针对宿主细胞的抗病毒手段仍有待探索。
2022年1月13日,南方科技大学田瑞琳实验室与美国加州大学旧金山分校(UCSF)Martin Kampmann实验室在Nature Cell Biology发表了题为“BRD2 inhibition blocks SARS-CoV-2 infection by reducing transcription of the host cell receptor ACE2”的文章,通过大规模CRISPR筛选鉴定出BRD2作为宿主细胞中潜在的抗新冠靶点。

新冠病毒感染宿主细胞主要依赖刺突蛋白的RBD结构域。使用体外纯化的RBD蛋白,研究人员从多种细胞系中鉴定出人肺腺癌细胞系Calu-3具有特异的RBD结合曲线,且结合依赖于Calu-3细胞中ACE2的表达,因此选择Calu-3进行后续研究。
为了系统性鉴定出宿主细胞中调控病毒感染的关键因子,研究人员在Calu-3细胞中以RBD的结合为表型进行了大规模CRISPRi筛选,筛选使用的sgRNA文库包含了所有已知的药物靶点基因(下图)。
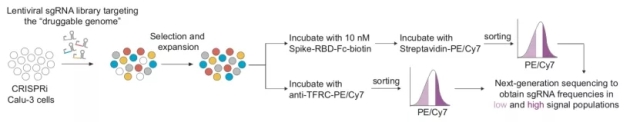
通过筛选,研究人员意外发现敲低BRD2基因可以有效抑制RBD结合。BRD2属于BET蛋白家族, 可以结合乙酰化修饰的组蛋白,调控基因转录。抑制BRD2的小分子药物如JQ1和ABBV-744已经在治疗癌症等其他疾病的临床试验中。
为了进一步验证抑制BRD2的抗病毒效果,研究人员在人原代支气管上皮细胞、人诱导多能干细胞分化的心肌细胞、人鼻粘膜上皮模型以及仓鼠体内模型中进行SARS-CoV-2活病毒感染,发现使用遗传学手段或者小分子抑制BRD2都可以非常显著地抑制病毒的感染增殖,且没有细胞毒性,说明BRD2是有效的抑制新冠病毒靶点。
抑制BRD2是如何阻止病毒感染增殖的?研究人员针对这一问题进行了下游的机制分析。研究人员发现,抑制BRD2可以几乎完全抑制宿主ACE2受体的mRNA转录。通过CUT-&-RUN,RNA-seq等后续实验,研究人员发现BRD2可以调控干扰素通路(interferon pathway)重要因子如STAT1, IRF9等的表达,而后者又可以控制ACE2的表达,因此抑制BRD2阻碍了interferon通路,从而抑制了ACE2的表达。
这项研究提示宿主细胞BRD2可以作为潜在的抑制新冠病毒感染的靶点,同时揭示了BRD2调控ACE2受体表达的机制。另外,这项研究也展示出基于CRISPR的遗传筛选技术在鉴定致病微生物治疗靶点的强大作用。
(来源:BioArt)
原文出处:Samelson, A.J., Tran, Q.D., Robinot, R. et al. BRD2 inhibition blocks SARS-CoV-2 infection by reducing transcription of the host cell receptor ACE2. Nat Cell Biol (2022). https://doi.org/10.1038/s41556-021-00821-8
链接:https://www.nature.com/articles/s41556-021-00821-8
