公共卫生学术热点追踪
Nature | 慢性肝损伤可诱导上皮可塑性的获得
动物的成年器官具有再生能力,不同的损伤诱导了不同的再生过程。然而,由于技术和伦理原因,对于许多成年人体器官,慢性疾病期间的组织再生成为了一个有争议的话题,因此,很难证明人类器官中存在此类事件。
肝脏乃代谢之重器,是在再生方面特别有趣的器官,在急性损伤后表现出显著的再生能力。肝上皮的主要功能细胞类型是肝细胞,胆管细胞排列在胆管树中并运输胆汁酸。这些细胞在损伤后被替换的过程取决于所受到的损伤。急性肝损伤期间会发生细胞增殖,但这种增殖能力在慢性疾病中会消失。
这其中的机制是什么?动物研究提示了三种可能机制:干细胞或祖细胞被激活后分化为上皮细胞;胆管细胞可以转分化为肝细胞,反之亦然;肝细胞和胆管细胞可以逆转为发育祖细胞,以恢复相应的细胞区室。这些机制在人类身上有迹可循,但人类慢性肝病期间发生的再生过程的性质仍有待充分了解。
为了针对人类肝脏解决这一难题,近日,来自英国剑桥大学的Michael Allison、Irina Mohorianu和Ludovic Vallier研究小组与德国、英国、希腊多国研究机构合作在Nature杂志上发表题为Acquisition of epithelial plasticity in human chronic liver disease的研究论文,这篇文章结合了单核分析、3D成像和功能实验来研究细胞行为和代谢功能障碍相关脂肪性肝病(MASLD)这种影响全世界海量人群的慢性肝病进展过程中发生的再生过程,结果表明慢性肝损伤创造了一种诱导人体器官细胞可塑性的环境,这篇文章为了解这一过程的潜在机制从而为慢性疾病的管理开辟了新的潜在途径。

MASLD是一种进行性疾病,始于肝细胞中脂肪的积累。随着时间的推移,这种积累会导致细胞死亡,进而导致炎症、纤维化、肝硬化和肝衰竭或肝癌。作者首先评估了受进行性MASLD影响的肝脏是否显示出再生过程,胆管细胞标志物角蛋白7(K7,也称KRT7)和角蛋白19(K19,也称KRT19)的免疫染色表明存在结合肝细胞和胆管细胞表型的细胞,这种双表型细胞与再生过程有关,因此它们的出现可能指示终末期MASLD的上皮再生。
为了进一步研究导致双表型细胞出现的事件及其在疾病中的作用,作者在单细胞水平上研究了MASLD的进展。为此,作者对47名MASLD进展不同阶段的人的肝脏进行了活检并进行了单核RNA测序(snRNA-seq)(图1)。集富集了肝细胞(n=69426)和胆管细胞(n=5412)。值得注意的是,肝细胞在疾病进展后显示出明显的转录变化,因此,肝细胞似乎是受该疾病影响最大的细胞类型,有共表达肝细胞和胆管细胞标志物的细胞存在。因此,双表型细胞的存在与进行性MASLD患者肝脏的再生过程有关。
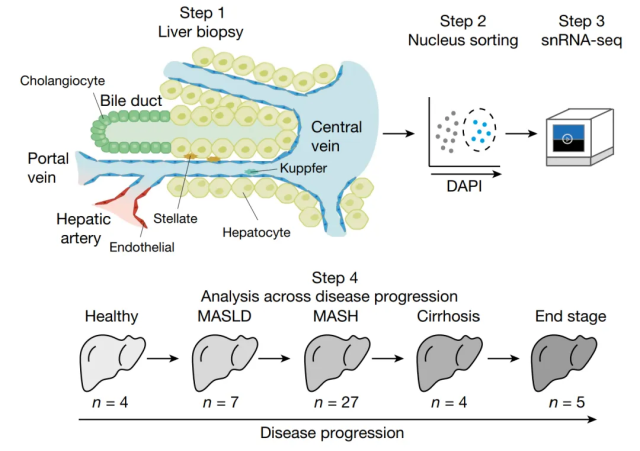
图1:snRNA-seq实验工作流程示意图。
免疫染色和抗体染色全器官(FLASH)成像的3D快速光显微镜分析表明疾病进展强烈改变了肝脏微环境,导致功能分带的丧失,MASLD进展过程中胆管数量增加,健康组织的K7染色显示了形成树枝状结构的导管网络,终末期样品在肝细胞结节周围表现出复杂的篮状结构,这样的结构表明胆管树发生了重塑(图2),在疾病进展过程中,双表型细胞的出现可能与胆管树和肝脏微环境的主要重组有关。
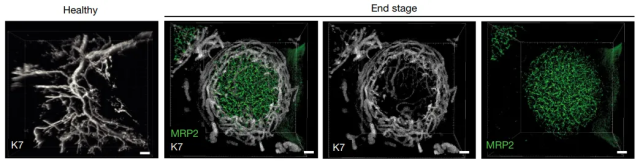
图2: K7染色。
在确定了双表型细胞的存在及其与疾病期间胆管树异常组织的部分联系后,作者接下来重点通过对肝细胞和胆管细胞进行详细的亚聚类来确定其起源。表达最高水平胆管细胞标志物的肝细胞在终末期疾病中更常见,表明细胞可塑性可能随着疾病进展而发生。双表型细胞出现在疾病进展过程中,而转分化在终末期疾病中很突出。
由于终末期细胞中标记物共表达达到了最高水平,因此作者通过终末期细胞来研究可塑性增加的机制,桥接胆管细胞和肝细胞的双表型细胞处于转分化状态。胆管细胞样肝细胞显示双向性,而肝细胞样胆管细胞显示从胆管细胞到肝细胞的方向。因此,转分化似乎是双向发生的。
PI3K–AKT信号与肥胖和代谢综合征有关,作者使用肝内胆管细胞类器官(ICOs)来验证PI3K–AKT信号的重要性。在mTOR抑制剂雷帕霉素、PI3K抑制剂LY294002和copanlisib以及AKT抑制剂MK2206存在下分化的ICO显示出肝细胞标志物表达的强烈降低。在mTOR激活剂MHY1485存在下,ICO的分化增强,表明该途径可以增加胆管细胞中肝细胞标志物的表达(图3)。mTOR–PI3K–AKT通路可能是胆管细胞分化为双表型细胞所必需的,在疾病进展过程中增加的循环胰岛素可能通过PI3K–AKT–mTOR途径在诱导肝上皮可塑性方面发挥关键作用。然而,可塑性的获得是渐进的,只有在肝脏微环境发生重大变化后才会发生。
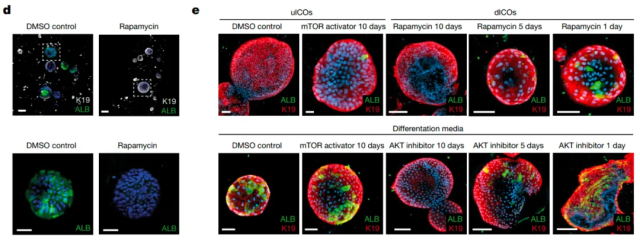
图3:PI3K–AKT–mTOR通路验证。
综上所述,这项研究对来自不同阶段代谢功能障碍相关脂肪肝患者的47例肝活检进行了snRNA-seq,建立了疾病进展过程中的肝脏细胞图谱,发现胆管细胞和肝细胞之间的细胞可塑性随着疾病的进展而增加,最终在终末期疾病中达到顶峰。更重要的是,这项研究揭示了肝细胞和胆管细胞之间发生的转分化事件,不需要成人干细胞或发育祖细胞激活,PI3K–AKT–mTOR通路在调节胆管细胞向肝细胞转分化中发挥重要作用,这个作用与胰岛素抵抗有关。
总之,人类上皮细胞可塑性的获得可能涉及多种信号和长期微环境的改变,未来更深入地了解控制可塑性出现的信号,将会为开发有效、安全的慢性肝病治疗策略铺平道路。
(来源:BioArt)
原文出处:Gribben C, Galanakis V, Calderwood A, Williams EC, Chazarra-Gil R, Larraz M, Frau C, Puengel T, Guillot A, Rouhani FJ, Mahbubani K, Godfrey E, Davies SE, Athanasiadis E, Saeb-Parsy K, Tacke F, Allison M, Mohorianu I, Vallier L. Acquisition of epithelial plasticity in human chronic liver disease. Nature. 2024 Jun;630(8015):166-173. doi: 10.1038/s41586-024-07465-2. Epub 2024 May 22. PMID: 38778114; PMCID: PMC11153150.
链接:https://pubmed.ncbi.nlm.nih.gov/38778114/
