公共卫生学术热点追踪
《Nature Communications》发表了非洲猪瘟病毒转录调控的分子机制
近日,兰州大学动物医学与生物安全学院/中国农业科学院兰州兽医研究所联合中国科学院生物物理研究所在《Nature Communications》期刊发表题为“Structural basis of RNA polymerase complexes in African swine fever virus”的研究论文,揭示了非洲猪瘟病毒(ASFV)RNA聚合酶(RNAP)复合体及其与转录泡结合的三维结构,为理解ASFV的转录周期及疫苗和药物研发提供了新思路。

非洲猪瘟是危害世界养猪业已逾百年的“头号杀手”,它是由ASFV感染家猪和野猪引起的一种急性烈性传染病,严重危害世界养猪产业。ASFV作为核质大DNA病毒,类似于牛痘病毒,自身可以编码与真核生物同源的RNAP核心亚基与转录因子,而不依赖宿主细胞完成转录过程。RNAP复合体作为ASFV生命周期关键的多功能蛋白质机器,负责基因组的转录和调控,研究其结构和功能意义重大。然而,由于组成RNAP复合体的亚基众多、不同转录状态其组成和构象会动态变化,ASFV转录调控的分子机制仍然尚不清楚。
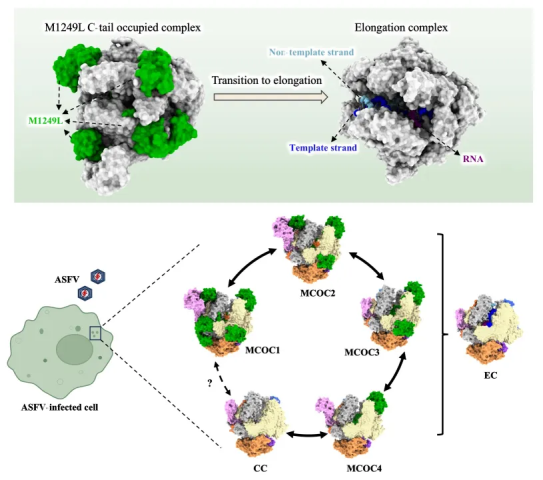
图:非洲猪瘟病毒内源RNA聚合酶复合体及延伸复合体结构
本研究利用亲和标签和蔗糖密度梯度离心纯化了感染状态下的内源ASFV RNAP,解析了多种天然构象的高分辨率冷冻电镜结构。此外,利用ASFV早期转录基因片段模拟转录泡结构,获得了转录延伸状态下的构象。体外功能实验表明,内源ASFV RNAP可以利用转录泡在体外延伸引物链。ASFV RNAP与经典RNAP的核心结构相似,但在外表面有一些独特的区域,可能介导与特定转录因子的相互作用。尤其是发现了一个独特的亚基M1249L,其结构类似于一个“笼子”,将核心亚基包裹在里面,与核心亚基形成了广泛的相互作用,稳定ASFV RNAP的整体结构。M1249L由多个结构域组成,与核心亚基动态结合,形成了多种构象,不同构象间可能互相转换,代表着不同的转录状态。M1249L C末端结构域深深地插入RNAP内部,占据了核酸结合位点。与牛痘病毒RNA聚合酶全复合体的结构分析表明,M1249L的结合导致多种经典转录因子的结合受阻。因此,M1249L作为ASFV特有的转录因子,稳定ASFV RNAP的整体结构,并通过动态结合机制调控ASFV RNAP的活性。这些研究结果不仅发现了天然状态下ASFV RNAP独特的结构特征,还为ASFV防控疫苗和药物的研发提供了理论基础。
近期,来自中国科学院生物物理研究所王祥喜、饶子和团队联合中国农业科学院哈尔滨兽医研究所步志高团队在《Nature Communications》发表了相近工作,共同为深入理解非洲猪瘟的致病机制提供了新的视角。
朱国梁青年研究员、席飞博士研究生和曾吴瑕硕士研究生为文章的第一作者,郑海学研究员、孙飞研究员、朱紫祥研究员和朱赟研究员为文章的通讯作者。该研究得到了国家重点研发计划项目、国家生猪产业技术体系、农科院项目、甘肃省项目、广东省项目等资助。
(来源:病毒学界)
原文出处:Zhu G, Xi F, Zeng W, Zhao Y, Cao W, Liu C, Yang F, Ru Y, Xiao S, Zhang S, Liu H, Tian H, Yang F, Lu B, Sun S, Song H, Sun B, Zhao X, Tang L, Li K, He J, Guo J, Zhu Y, Zhu Z, Sun F, Zheng H. Structural basis of RNA polymerase complexes in African swine fever virus. Nat Commun. 2025 Jan 8;16(1):501. doi: 10.1038/s41467-024-55683-z. PMID: 39779680; PMCID: PMC11711665.
