公共卫生学术热点追踪
Nat Microbiol | 同济大学戈宝学等发现结核杆菌上调调节性T细胞CTLA-4抑制宿主抗结核免疫
调节性T (Treg)细胞在结核分枝杆菌(Mtb)感染期间扩增,并抑制T细胞介导的控制。Mtb是否积极参与了这一过程尚不清楚。
2025年10月10日,同济大学戈宝学、杨华、季哲及中国医学科学院北京协和医学院孙义成共同通讯在Nature Microbiology(IF=19.4)在线发表题为“Mycobacterium tuberculosis-derived linoleic acid increases regulatory T cell function to promote bacterial survival within macrophages”的研究论文,该研究表明结核分枝杆菌衍生的亚油酸增加调节性T细胞功能以促进巨噬细胞内的细菌存活。

结核分枝杆菌(Mtb)使用许多复杂的策略来抵抗或削弱无数的巨噬细胞防御,以提高其细胞内存活率,使其能够在肺中持续存在和增殖。最近的研究表明,D-丝氨酸是Mtb在缺氧条件下产生的代谢产物,它选择性抑制T细胞(特别是CD8+ T细胞)产生干扰素-γ (IFNγ),从而消除T细胞对巨噬细胞抗菌能力的增强作用。然而,结核分枝杆菌是否以及如何操纵其他适应性免疫细胞来促进其感染仍有待阐明。
尽管调节性T (Treg)细胞通过抑制CD4⁺ T细胞反应来阻止结核分枝杆菌的根除,但由Treg细胞产生的免疫抑制性细胞因子白细胞介素-10 (IL-10)和转化生长因子-β(TGF-β)在这方面的作用似乎不太重要。相反,Treg细胞主要通过抑制关键细胞因子如IFNγ和白细胞介素-17 (IL-17)的产生来阻碍有效的抗分枝杆菌免疫,它们对控制结核杆菌感染至关重要。Treg细胞在感染结核分枝杆菌的患者中扩增,并抑制效应T细胞产生抗原特异性IFNγ。同样,在结核杆菌感染的小鼠中,Treg细胞扩张并限制肺部的细菌清除。此外,在这些感染小鼠中产生的Treg细胞延迟了效应T细胞在感染肺中的募集,延长了细菌扩张的初始阶段。然而,尚不清楚结核分枝杆菌是否以及如何利用Treg细胞来调节巨噬细胞的抗菌能力。
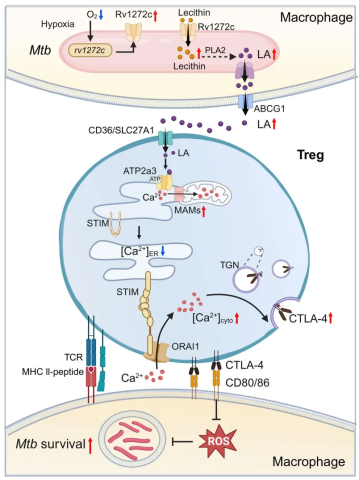
机理模式图(图源自Nature Microbiology)
作为一种关键的免疫检查点分子,细胞毒性T淋巴细胞抗原4 (CTLA-4)在Treg细胞上高度组成性表达,并介导关键的免疫抑制功能,包括配体表达的下调和抑制信号的传递。已有研究表明,CTLA4基因的遗传多态性与结核病易感性相关。与健康对照相比,潜伏性结核病患者淋巴细胞中的CTLA-4水平较高。在结核杆菌感染小鼠的肺淋巴结中,结核杆菌特异性Treg细胞的细胞表面CTLA-4表达高于foxp3-常规CD4⁺ T细胞。然而,CTLA-4在介导对结核分枝杆菌感染的免疫反应中的功能仍不清楚。
在该研究中,研究人员表明Mtb Rv1272c(一种ATP结合盒转运蛋白)的表达在缺氧条件下增加,并通过增加卵磷脂的输入,随后产生和释放亚油酸来促进Mtb在体内的存活。被感染的巨噬细胞释放的亚油酸通过Ca2+转运蛋白ATP2a3促进Treg细胞中免疫检查点分子细胞毒性T淋巴细胞抗原4 (CTLA-4)的表面运输。这反过来抑制了巨噬细胞活性氧的产生,并促进了巨噬细胞内结核分枝杆菌的存活。Rv1272c诱导的亚油酸通过增加体内Treg细胞上CTLA-4表面运输进一步促进Mtb免疫逃避。在机制上,亚油酸与Treg细胞中的ATP2a3相互作用,并促进线粒体相关的内质网(ER)膜形成。这促进了内质网到线粒体的Ca2+转移和内质网中Ca2+的耗竭,并触发了储库操纵的钙进入,从而提高了胞质Ca2+水平,增加了Treg细胞中Ca2+依赖的CTLA-4表面运输。这些发现揭示了结核分枝杆菌可以利用代谢物来操纵宿主反应并促进其细胞内存活。
(来源:iNature)
原文出处:Cheng H, Li S, Liu H, Yan M, Wang J, Huang J, Liu S, Yang Y, Cao X, Cui P, Cheng Y, Liu Z, Wang J, Huang X, Wang L, Qin L, Zheng R, Feng CG, Zou Q, Sun Y, Ji Z, Yang H, Ge B. Mycobacterium tuberculosis-derived linoleic acid increases regulatory T cell function to promote bacterial survival within macrophages. Nat Microbiol. 2025 Oct 10. doi: 10.1038/s41564-025-02140-2. Epub ahead of print. PMID: 41073667.
