公共卫生学术热点追踪
Cell Reports:浙江大学徐平龙/华南农业大学黄耀伟合作揭示戊肝病毒ORF3相分离功能
HEV是一种单链正义RNA病毒,为人畜共患病原体,可引起急性或慢性肝炎,尤其对孕妇和免疫低下人群危害严重。HEV基因组包含3个开放阅读框(ORF1-3),其中编码蛋白pORF1负责病毒RNA复制,pORF2构成病毒衣壳,而pORF3对病毒体内感染必需、具有介导准囊膜HEV(eHEV)的组装与释放、拮抗宿主天然免疫、调控细胞代谢等多种功能。液-液相分离(LLPS)是生物大分子通过自发相分离形成无膜细胞器(Membraneless Organelles, MLOs)的物理过程,其核心驱动因素包括分子间多价相互作用及细胞微环境调控。近年来多项研究发现病毒利用LLPS实现生命周期的多个关键步骤,包括入侵、复制、组装及免疫逃逸。脂滴(LDs)是动态细胞器,储存甘油三酯(TAG)和胆固醇酯(CE)等中性脂质,参与能量代谢和膜合成,也已报道与新冠病毒、丙肝病毒、登革病毒等多种病毒的生命周期密切相关。然而,HEV感染周期与肝脂代谢及脂滴生成的相互作用还未受到关注。
近日,浙江大学徐平龙与华南农业大学黄耀伟有关研究团队合作,在Cell Reports 上发表题为pORF3-Driven Biogenesis of Lipid Droplets Facilitates HEV Infectivity的研究工作(Cell Reports, 2025, doi.org/10.1016/j.celrep.2025.116406),该研究从肝脏脂代谢和脂滴生物学以及细胞液-液相分离是否参与HEV生命周期,病毒蛋白pORF3如何实现其多种HEV病-宿互作功能等核心科学问题为出发点,最终发现一条独特的“pORF3-LLPS-LD”轴,串联诠释了以上的部分未知空白,为理解HEV生命周期及病宿互作全景提供全新的视角。

研究发现在细胞模型和沙鼠动物模型中,HEV感染诱导显著的肝细胞脂滴生成,包括脂滴数量和大小显著增加,且脂滴水平与病毒滴度呈正相关。临床表型上,高脂饮食组沙鼠肝脏HEV RNA拷贝数和粪便病毒载量较普通饮食组增加1.5-2倍,且肝脏脂滴消耗增加。敲除ORF3后, HEV突变株无法诱导脂滴生成,病毒滴度显著降低,表明pORF3是脂滴生成的关键驱动因子。机制上,pORF3通过其56-76位氨基酸的内在无序区域(IDR)发生LLPS,形成具有流动性的凝聚物,与脂滴表面结合并诱导“pORF3核心-脂质外壳”的独特结构,从而调控脂滴生物发生。pORF3通过LLPS凝聚物与胆固醇合成通路相互作用,显著上调关键合成基因的表达,促进脂滴主要成分TAG和CE合成;另一方面,HEV感染消耗肝细胞脂滴(通过释放eHEV至胞外),而pORF3持续诱导脂滴生成以维持病毒复制或组装需求,形成“消耗-再生”循环。值得注意的是,使用降脂药物阿托伐他汀抑制胆固醇合成,或者反向遗传技术敲除病毒ORF3,都可以显著减少肝细胞脂滴含量,降低HEV RNA拷贝数和病毒释放,并在体内外有效抑制HEV感染。工作揭示了脂代谢在HEV病宿互作中的重要作用,也表明抑制脂滴生成可能是有效阻断HEV感染抗病毒干预新策略 (图),或为慢性HEV患者提供潜在的治疗方案。
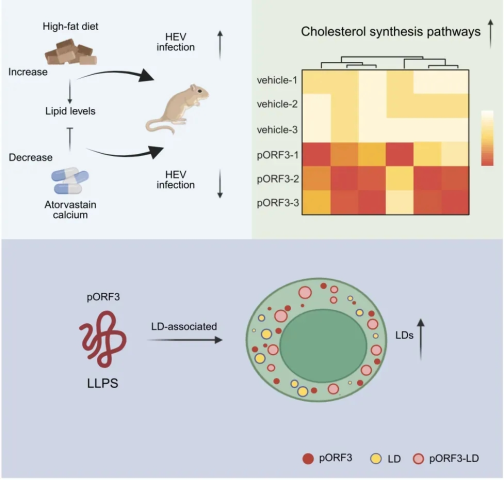
本研究重新审视并凸显pORF3在HEV的体内真实感染周期全过程中的关键作用,初步阐明肝细胞脂滴的生物形成受病毒pORF3蛋白引发的LLPS所驱动,这是LLPS与脂滴的生物合成及功能重塑直接关联的首次报道。工作揭示了脂滴代谢是HEV感染肝脏的关键枢纽之一,可能为HEV在感染细胞的“病毒工厂”提供能量、复制场所,以及准囊膜病毒粒子(eHEV)的脂质囊膜来源,因此为病毒如何劫持宿主脂类代谢通路提供了一个新范例。
此前本文通讯作者之一的黄耀伟教授在博士后期间(2007年)报道了猪HEV ORF3缺失突变株丧失对猪的感染能力。“pORF3-LLPS-LD”轴的发现提示pORF3不仅介导之前报道的eHEV的形成与释放,还由于其具备形成相分离凝聚体的特征,可能扮演着HEV病毒工厂的“组织者”角色。从这一角度或可解释pORF3为何是一种多功能蛋白:没有pORF3凝聚体与细胞不同组分(包括LDs)的互作动态地调控宿主微环境,HEV将无法在动物体内产生具有感染性的子代或具备感染能力。因此,本研究工作的另一重要科学意义在于,通过pORF3凝聚体的发现,为诠释HEV生命周期动态全景提供了新见解,有望以LLPS为框架偶联起不同的HEV分子病毒学事件。
浙江大学生命科学研究院徐平龙教授、华南农业大学兽医学院/动物疫病防控全国重点实验室黄耀伟教授、浙江大学生命科学研究院叶存奇教授、浙江大学医学院附属第一医院梁廷波教授为论文的共同通讯作者。浙江大学实验动物中心徐令东高级工程师、浙江大学杭州国际科创中心张飞研究员和浙江大学生研院博士生缪灿为论文的共同第一作者。
(来源:生命科学前沿、BioArt、病毒学界)
原文出处:Xu LD, Zhang F, Miao C, Yu X, Zhu Y, Zhang MD, Liu S, Sridhar S, Sun Q, Neculai D, Zhang Q, Shen L, Liang T, Ye C, Huang YW, Xu P. pORF3-driven biogenesis of lipid droplets facilitates HEV infectivity. Cell Rep. 2025 Oct 8;44(10):116406. doi: 10.1016/j.celrep.2025.116406. Epub ahead of print. PMID: 41066231.
