公共卫生学术热点追踪
Nature子刊 | 梁兴杰/滕皋军开发新型纳米药物,预防急性血栓形成
抗血小板药物是治疗血栓形成高危患者的一个里程碑。然而,它们的临床应用仍然受到出血相关风险和有限疗效的限制。由受损的血管内皮细胞产生的过量活性氧(ROS)已经显示出刺激血栓形成。
2025年10月31日,国家纳米科学中心梁兴杰、东南大学滕皋军共同通讯在Nature Nanotechnology(IF=35.1)在线发表题为“Prevention of acute thrombosis with vascular endothelium antioxidative nanoscavenger”的研究论文,该研究提出一种由黑色素和过氧化氢酶交联形成的ROS趋化纳米颗粒(MDCP ),通过保护血管内皮细胞免受氧化应激而预防急性血栓形成。
研究人员证明,MDCP治疗抑制活性氧诱导的内皮细胞凋亡,从而维持内皮细胞的完整性,防止胶原暴露,从而防止血小板活化和血栓形成。通过避免直接干扰血小板功能,这种通过MDCP调节血管氧化还原稳态的方法提供了一种有前途的替代抗血栓策略,解决了目前临床抗血栓药物的出血风险。

急性动脉血栓形成是全球高发病率和死亡率的主要原因。在临床实践中,抗血小板治疗是一种广泛用于血栓形成高危患者的预防策略,如动脉粥样硬化、糖尿病或高血压患者,以及接受过经皮冠状动脉介入治疗的患者。然而,目前的抗血小板药物,包括阿司匹林和氯吡格雷,有出血的风险,因为它们阻断了血小板的活化,这是生理止血的关键过程。同时,一些接受长期阿司匹林治疗的患者出现耐药性,这可能导致残余心血管事件。靶向给药已被用于特异性抑制活化血小板而非静止血小板,从而有效防止血栓形成,而不增加出血风险。然而,独立于抗血小板途径的急性动脉血栓预防策略很少被研究。
活性氧(ROS)的产生和消除之间的动态平衡维持了代谢稳态。血管损伤会提高活性氧的水平,如超氧阴离子(O2-.)和过氧化氢(H2O2),从而增加血栓形成的风险。这种异常的生理信号已被用作一种刺激,在血管损伤部位触发ROS反应性药物释放,用于抗血栓治疗。此外,抗氧化剂已被用于减轻缺血-再灌注损伤或辅助抗血栓药物预防继发性血栓形成。然而,目前尚不清楚是否可以通过直接清除损伤血管中过量的ROS来预防急性血栓形成。
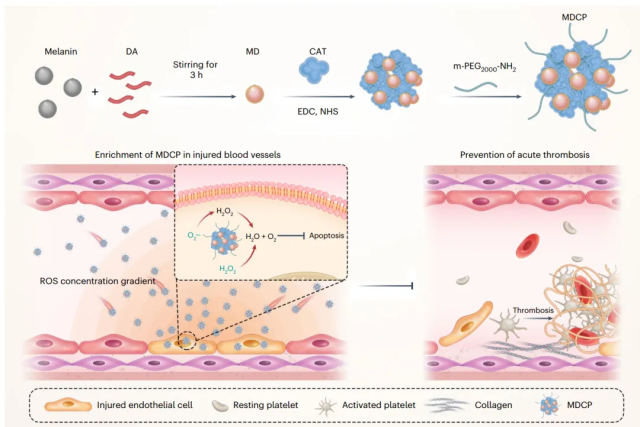
机理模式图(图源自Nature Nanotechnology )
此外,血流的高剪切应力对受伤部位的药物快速积累构成了挑战。值得注意的是,血管损伤后,受损内皮细胞中的ROS水平显著增加,加剧了其凋亡和与血管基质的分离。暴露于内皮下基质后,循环血小板被血管性血友病因子募集到损伤部位,随后被胶原蛋白激活,开始聚集,最终导致血栓形成。因此,通过清除受损血管中过量的ROS来保护内皮细胞为预防急性血栓形成提供了一种潜在的策略。
在这里,研究人员提出一种ROS趋化纳米粒子(MDCP),整合了过氧化氢酶(CAT)和黑色素的天然酶特性,通过保护内皮细胞免受氧化应激来预防急性血栓形成。预先注射的MDCP可以通过活性氧梯度诱导的酶趋化性在受损血管中特异性富集,并以酶活性依赖的方式清除过量产生的H2O2,同时伴有O2的催化分解。这一过程促进了参与一氧化氮(NO)和谷胱甘肽合成的抗氧化代谢物的上调,同时减少了炎症因子的释放。这些作用增强了内皮细胞对活性氧诱导的凋亡的抵抗力,从而防止了内皮下层胶原的暴露和随后的血小板活化。结合其对血小板功能的可忽略影响,这种MDCP介导的血管氧化还原稳态调节提供了一种安全和有前途的抗血栓形成替代方案。
(来源:iNature)
原文出处:Zhong Y, Ni Q, Huang L, Qing G, Zhang F, Gong N, Wu H, Liao Y, Jiang H, Tu Z, Wang Z, Jiramonai L, Zhu H, Teng GJ, Liang XJ. Prevention of acute thrombosis with vascular endothelium antioxidative nanoscavenger. Nat Nanotechnol. 2025 Oct 31. doi: 10.1038/s41565-025-02046-4. Epub ahead of print. PMID: 41174280.
