公共卫生学术热点追踪
Science | 虽然“长得丑”,但是“很有用”!多系统的蝙蝠类器官模型为人畜共患病毒提供高质量的病理生理模型
蝙蝠是人畜共患病病原体的重要宿主,但用于全面探究宿主与病原体相互作用以及评估溢出风险的合适模型系统仍然有限。
2025年5月15日,韩国基础科学研究所Young Ki Choi团队在Science 在线发表题为“Diverse bat organoids provide pathophysiological models for zoonotic viruses”的研究论文,为填补这一空白,该研究开发了一系列涵盖五种物种和横跨四种器官类型的蝙蝠类器官培养模型。
这个多物种、多器官的类器官培养模型显示了针对几种病毒的物种和组织特异性复制模式,为研究呼吸道、肾脏和肠道的人畜共患病病毒提供了可靠的病理生理模型。利用这个平台,该研究成功分离并鉴定了蝙蝠传播的哺乳动物正冠病毒和副粘病毒,证明了这些组织培养模型在病毒组监测中的实用性。此外,该研究还成功测试了已知的抗病毒药物对蝙蝠病毒分离株的疗效。

世界卫生组织将人畜共患疾病定义为任何能够从脊椎动物自然传播至人类的疾病或感染。从历史上看,许多大流行病,如黑死病、西班牙流感和新冠肺炎,都源自人畜共患病原体。据估计,人类新出现或正在流行的约 75%的传染病都源于人畜共患病毒。
蝙蝠似乎是几种人畜共患病毒的重要宿主动物,包括导致 SARS、MERS 和新冠肺炎的冠状病毒,以及亨尼帕病毒、狂犬病毒和丝状病毒。这些病原体的传播往往涉及中间宿主,它们有助于弥合蝙蝠和人类之间的生态和分子鸿沟。随着气候变化的持续以及人类向野生动物栖息地的侵入,分隔蝙蝠和人类的自然生态屏障正在减少,从而增加了病毒溢出的风险。
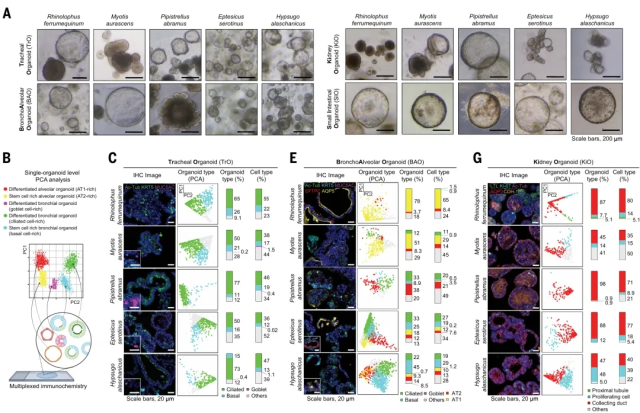
建立并鉴定多物种、多器官的蝙蝠类器官模型,用于生物样本库的建立以及同时监测蝙蝠病毒组(图源自Science )
尽管蝙蝠传播的病毒构成了明显的威胁,但目前用于研究这些病原体的生理学模型是有限的。通过宏基因组研究鉴定出的大多数蝙蝠病毒尚未被分离出来,主要原因在于缺乏适合培养这些病毒的蝙蝠模型系统。目前所存在的代表蝙蝠呼吸道和胃肠道上皮的组织体模均是从热带果蝠中获得的。这些区域和物种的特殊性限制了它们在全球人畜共患病研究中的适用性。
为填补这一空白,研究人员从属于翼手目的四个东亚食虫蝙蝠物种(包括一种属于鼻蝠科的物种)中建立了多物种、多器官上皮类器官。后者此前已被用于建立肠道类器官。类器官集合涵盖了气管、肺、肾脏和小肠,为实验研究蝙蝠上皮组织的生理特征提供了途径,同时也可作为病毒组监测、病原体分离以及药物测试的平台。
(来源:iNature)
原文出处:Kim H, Heo SY, Kim YI, Park D, N MPA, Hwang S, Lee YK, Jang H, Ahn JW, Ha J, Park S, Ji HY, Kim S, Choi I, Kwon W, Kim J, Kim K, Gil J, Jeong B, Lazarte JCD, Rollon R, Choi JH, Kim EH, Jang SG, Kim HK, Jeon BY, Kayali G, Webby RJ, Koo BK, Choi YK. Diverse bat organoids provide pathophysiological models for zoonotic viruses. Science. 2025 May 15;388(6748):756-762. doi: 10.1126/science.adt1438. Epub 2025 May 15. PMID: 40373131.
