公共卫生学术热点追踪
Science | 人体内早有“防火墙”!浙江大学于晓方/吉林大学魏伟团队合作揭示STING蛋白如何阻止禽流感传入,但病毒已进化出“钥匙”
流感大流行通常源于禽流感 A 病毒(IAV)向人类的传播。然而,阻止 IAV 传播的屏障仍未被明确。
2026年2月26日,浙江大学于晓方团队及吉林大学魏伟团队合作在Science 在线发表题为“STING–NF-κB signaling builds an influenza spillover barrier”的研究论文,该研究发现人类干扰素刺激基因(STING)是抵御 IAV 的屏障。STING 通过特定区域激活核因子κB(NF-κB)以及下游的 NF-κB 诱导基因(NSGs)。在这些 NSGs 中,生长停滞和 DNA 损伤诱导蛋白 34(GADD34)对于 IAV 的抑制至关重要。
一些 IAV 已经进化出通过改变其基质蛋白 1(M1)中的第 115 个残基来逃避激活人类 STING 的机制,而该残基对于病毒在人类呼吸道细胞中的高效复制是必不可少的。这种抵御 IAV 从动物传播到人类这一威胁的屏障,为未来对环鸟苷单磷酸-腺苷单磷酸(cGMP-AMP)合酶(cGAS)-STING-NF-κB 信号通路的生物学功能的研究提供了工具。
源自禽类的甲型流感病毒(IAV)一直构成着持续的全球性疫情威胁。要实现传播,禽类 IAV 必须适应并克服人类细胞的防御机制。尽管已经发现了若干保护屏障,例如受体兼容性和聚合酶适应性等,但人类细胞的防御机制的全貌仍不完全清楚。禽类 IAV 能够有效地避开人类的 RNA 感应途径,但它们在人类细胞中的复制能力仍然有限。这种现象表明,人类固有免疫系统的其他组成部分可能作为对抗禽类 IAV 的另一道屏障发挥作用。
通过运用药物学和遗传学方法,该研究确定 STING 通过激活核因子κB(NF-κB)通路来抑制甲型流感病毒(IAV)。对 STING 点突变库的进一步筛选表明,STING 中的 Gly90 残基对于激活 NF-κB 和抑制 IAV 复制至关重要。这一发现已在携带内源性 Gly90 敲入突变的原代人类呼吸细胞以及点突变小鼠中得到证实。
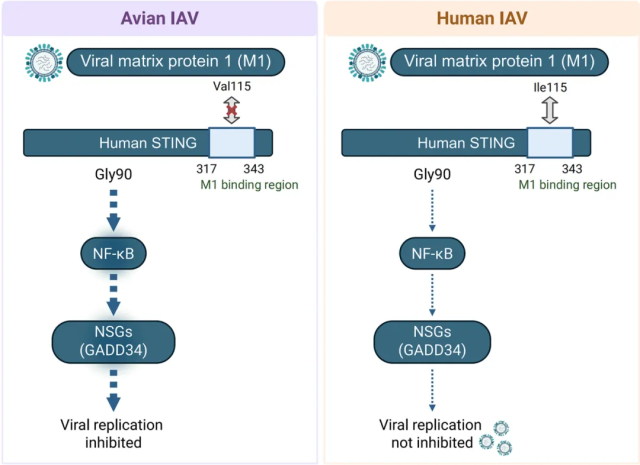
M1 蛋白的进化使甲型流感病毒能够突破 STING - NF-κB - GADD34 的抗病毒防线(图源自Science )
将过表达野生型 STING 引起的转录变化与 STING G90A(Gly90→Ala)突变引起的转录变化进行了比较,以确定候选的抗病毒 NF-κB 诱导基因(NSGs),并通过小干扰 RNA 筛选进行了验证。由此,该研究确定了生长停滞和 DNA 损伤诱导蛋白 34(GADD34),它在人类细胞中抑制了 IAV 复制。GADD34 主要在人类呼吸系统中表达,并独立于其常规的磷酸酶功能抑制 IAV 聚合酶活性。
对 IAV 编码蛋白的检测表明,人类 IAV 编码的基质蛋白 1(M1)蛋白能够介导对人类 STING–NF-κB–GADD34 通路的逃避。该研究发现,来自禽类 IAV 的 M1 蛋白在对抗人类 STING 方面的效果不如人类 IAV 的 M1 蛋白,尽管它对禽类 STING 仍具有完全的活性。序列比对发现 M1 蛋白第 115 位存在一个缬氨酸到异亮氨酸的替换,这一替换使得它能够特异性地逃避人类 STING(而非禽类 STING),从而增强了禽类特征的 IAV 在哺乳动物细胞中的复制能力。
总之,该研究提出,STING 可能起到一种“溢出屏障”的作用,以防止禽流感病毒向人类的传播。流感病毒 M1 蛋白中第 115 位残基从缬氨酸变为异亮氨酸的这种进化变化,可能在规避这一限制方面发挥着关键作用,并赋予病毒在人类细胞中复制的优势。因此,对 M1-115 变体的监测可以作为预测禽流感跨物种传播风险的分子标志物。此外,开发能够破坏 M1-STING 交互作用的药物,特别是针对含有异亮氨酸 115 的病毒株,能够增强应对未来流感大流行的准备能力。
(来源:iNature)
原文出处:Ye R, Wang S, Hu Y, Pan Y, Zheng W, Xia F, Wang Y, Guo H, Zheng S, Wei W, Yu XF. STING-NF-κB signaling builds an influenza spillover barrier. Science. 2026 Feb 26;391(6788):eads4405. doi: 10.1126/science.ads4405. Epub 2026 Feb 26. PMID: 41747053.
