公共卫生学术热点追踪
Nature Aging | 苏州大学团队揭示免疫衰老机制,提升老年疫苗效力
老龄化社会的免疫挑战
随着全球人口老龄化进程加速,如何提升老年人群的疫苗效力已成为公共卫生领域亟待解决的重大课题。衰老伴随着免疫系统功能的逐渐衰退,在新冠疫情期间,年龄成为导致重症综合征最关键的风险因素之一。尽管疫苗研发取得巨大成功,但老年人接种后通常表现出抗体反应减弱、效应T细胞应答下降以及免疫记忆形成受损。树突状细胞作为免疫系统中关键的抗原提呈细胞,在启动免疫应答中发挥着核心作用,然而,树突状细胞是否以及如何在衰老导致的疫苗反应减弱中发挥作用,此前尚未得到充分阐明。
关键发现:衰老相关树突状细胞迁移缺陷
苏州大学汪超教授、吴玉敏副研究员和中国医学科学院医学生物学研究所刘野课题组合作,通过单细胞RNA测序技术,对年轻和老年小鼠接种疫苗后的淋巴结变化进行了系统分析,首次发现衰老过程中树突状细胞存在迁移缺陷,并在迁移性树突状细胞中鉴定出与功能障碍相关的基因特征。更重要的是,研究团队证明口服酵母来源的纳米颗粒能够显著提升肠道树突状细胞趋化因子受体CCR7的表达,促进其在免疫后响应趋化信号向淋巴结迁移,从而增强衰老动物的疫苗诱导免疫应答。这一发现不仅揭示了免疫衰老的关键机制,还为改善老年人疫苗效力提供了一种非侵入性策略。相关论文以Restoring the tumour mechanophenotype of vocal fold cancer reverts its malignant properties为题,发表在nature aging。

老年小鼠疫苗应答减弱的实验验证
研究团队首先通过实验证实了老年小鼠确实表现出减弱的疫苗应答。研究人员对年轻(8-10周龄)和老年(80-90周龄)雌性C57BL/6J小鼠进行RBD蛋白皮下免疫,使用弗氏佐剂进行初次和加强免疫。实验结果显示,老年小鼠血清抗RBD IgG结合滴度显著低于年轻小鼠,对新冠病毒Wuhan、Beta、Delta和BA.1株的中和抗体滴度也明显降低。流式细胞术分析显示,老年小鼠淋巴结中生发中心B细胞数量减少,脾细胞中IFNγ产生细胞显著减少,CD4+和CD8+ T细胞中IFNγ、IL-2和TNF的产生频率均明显下降(图1)。这些结果证实了衰老确实削弱了疫苗诱导的体液免疫和细胞免疫应答。
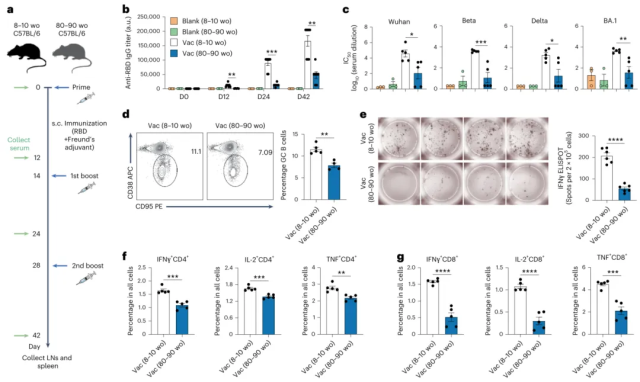
图1 | 老年小鼠表现出减弱的疫苗免疫应答。 a,年轻(8-10周龄)和老年(80-90周龄)C57BL/6J小鼠RBD蛋白疫苗接种实验时间线。RBD蛋白与弗氏佐剂乳化后皮下注射于小鼠腹部(初次免疫用完全佐剂;加强免疫用不完全佐剂)。未接种年轻对照组,空白(8-10周龄);未接种老年对照组,空白(80-90周龄);接种年轻小鼠,Vac(8-10周龄);接种老年小鼠,Vac(80-90周龄)。b,ELISA检测血清抗RBD IgG结合滴度(空白(8-10周龄)、空白(80-90周龄),n=4;Vac(8-10周龄)、Vac(80-90周龄),n=8,生物学重复)。P值(从左至右),P=0.0048,P=0.0006,P=0.0083。c,第42天测量的针对Wuhan、Beta、Delta和BA.1株的假型慢病毒中和抗体滴度(50%中和,IC50)(空白(8-10周龄)、空白(80-90周龄),n=3;Vac(8-10周龄)、Vac(80-90周龄),n=5,生物学重复)。P值(从左至右),*P=0.0189,P=0.0009,*P=0.0163,P=0.0066。d,淋巴结中生发中心B细胞(CD95+CD38-CD19+CD45+)的流式细胞术分析(Vac(8-10周龄),n=5;Vac(80-90周龄),n=4,生物学重复)。P=0.0014。e,免疫后第50天通过ELISpot测定再刺激脾细胞的IFNγ斑点形成细胞及统计数据(每组n=6,生物学重复)。**P<0.0001。f,CD4+ T细胞中IFNγ、IL-2和TNF的频率(每组n=5,生物学重复)。P值(从左至右),*P=0.0002,P=0.0004,P=0.0021。g,CD8+ T细胞中IFNγ、IL-2和TNF的频率(每组n=5,生物学重复)。P值(从左至右),P<0.0001,P<0.0001,**P=0.0002。数据表示为均值±标准误。统计分析采用双尾Student t检验。
迁移性cDC2缺陷与疫苗反应降低相关
为进一步探究树突状细胞在衰老相关疫苗反应减弱中的作用,研究团队对年轻和老年小鼠免疫后的淋巴结进行了单细胞RNA测序分析。结果显示,老年小鼠淋巴结中迁移性常规树突状细胞2型的数量和频率显著低于年轻小鼠,而这种差异在其他树突状细胞亚群中并不明显。更重要的是,迁移性cDC2的减少与血清抗体滴度下降呈显著正相关(图2)。基因表达分析表明,老年小鼠迁移性cDC2中与抗原加工提呈、趋化信号通路相关的基因表达下调,而细胞功能障碍相关基因表达上调。这些发现提示迁移性cDC2缺陷可能是导致老年疫苗反应减弱的关键因素。
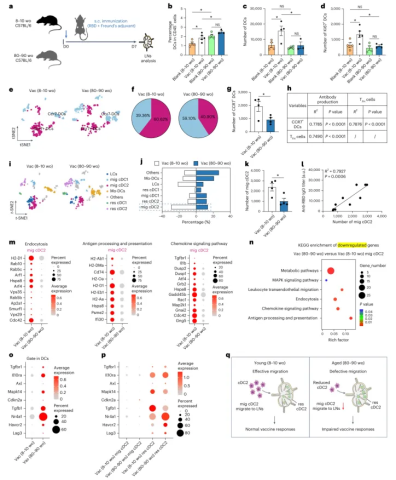
图2 | 淋巴结迁移性cDC2缺陷导致疫苗反应降低。 a,实验设计。b,t-SNE图显示年轻和老年小鼠接种疫苗后淋巴结免疫细胞的重新分组。c,不同树突状细胞亚群的t-SNE图。d,树突状细胞亚群代表性基因的小提琴图。e,迁移性cDC2(CD11b+XCR1-MHCII+CD11c+Epcam-CD45+)的代表性流式细胞术分析和定量结果(Vac(8-10周龄),n=5;Vac(80-90周龄),n=4,生物学重复)。*P=0.0208。f,迁移性cDC2绝对数量与血清抗RBD IgG结合滴度的相关性(n=22,生物学重复)。P<0.0001。g,代表性趋化因子信号通路基因在迁移性cDC2中的表达。h,KEGG富集分析显示老年小鼠迁移性cDC2中下调的通路。数据表示为均值±标准误。统计分析采用双尾Student t检验。
口服YNP恢复老年小鼠迁移性cDC2并增强疫苗应答
基于上述发现,研究团队探索了通过口服酵母纳米颗粒补充淋巴结迁移性cDC2的可能性。研究使用超高压低温均质法制备了约300纳米的酵母纳米颗粒,其主要成分为90.60%的β-葡聚糖,具有良好的稳定性和分散性。老年小鼠口服YNP一周后,淋巴结中树突状细胞的数量和频率显著增加,Ki67+增殖树突状细胞数量也明显上升。单细胞RNA测序和流式细胞术分析证实,YNP处理显著提高了老年小鼠淋巴结中CCR7+树突状细胞的比例和数量,特别是迁移性cDC2亚群显著增加(图3)。转录分析显示,YNP处理后迁移性cDC2中与内吞作用、抗原加工提呈和趋化信号通路相关的基因明显上调,而细胞功能障碍标志物表达下调。
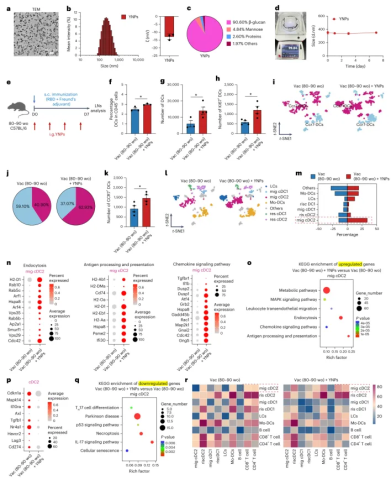
图3 | 口服YNP补充老年小鼠淋巴结迁移性cDC2。 a,酵母和YNP的扫描电镜图像。b,YNP的透射电镜图像。c,YNP的成分分析。d,YNP在磷酸盐缓冲液中随时间变化的稳定性。e,实验时间线。f,淋巴结中树突状细胞(CD11c+MHCII+CD45+)的代表性流式细胞术分析和定量结果(Vac(80-90周龄)n=3;Vac(80-90周龄)+YNP,n=4,生物学重复)。*P=0.0499。g,h,淋巴结中Ki67+树突状细胞的代表性流式细胞术分析和绝对数量(每组n=4,生物学重复)。*P=0.0218。i,j,t-SNE图和CCR7+和CCR7-树突状细胞的比例。k,淋巴结中CCR7+树突状细胞的代表性流式细胞术分析(每组n=4,生物学重复)。*P=0.0461。l,m,树突状细胞亚群分析的t-SNE图及相应的定量结果。n,迁移性cDC2中代表性基因表达的点图。o,迁移性cDC2中上调基因的KEGG富集分析。p,树突状细胞亚群中功能缺陷相关基因的表达比较。q,迁移性cDC2中下调基因的KEGG富集分析。r,树突状细胞亚群、B细胞、CD4+ T细胞和CD8+ T细胞间的细胞通讯分析。数据表示为均值±标准误。统计分析采用双尾Student t检验。
YNP显著提升老年小鼠疫苗免疫应答
研究进一步评估了口服YNP对老年小鼠疫苗应答的增强效果。老年小鼠在皮下免疫RBD蛋白的同时,每隔两天口服YNP,持续一周。结果显示,YNP处理使老年小鼠抗RBD IgG滴度比未处理免疫对照组提高了2.5至3倍,对多种新冠病毒株的中和抗体反应也显著增强(图4)。淋巴结分析表明,YNP处理显著增加了生发中心B细胞、滤泡辅助T细胞和浆细胞的数量。单细胞RNA测序显示,YNP处理后T细胞活化、TFH细胞分化和适应性免疫应答相关基因富集增强,B细胞活化、分化和增殖相关通路也明显上调。脾细胞ELISpot分析和细胞内细胞因子染色证实,YNP处理显著增强了抗原特异性T细胞免疫应答,恢复了T细胞的多功能性。
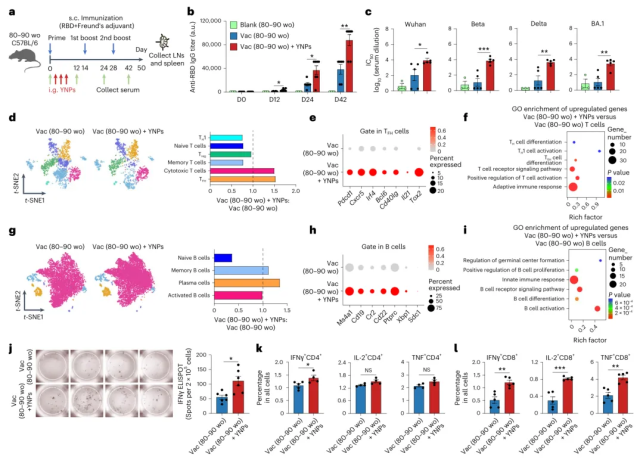
图4 | YNP增强老年小鼠的疫苗应答。 a,老年C57BL/6J小鼠(80-90周龄)免疫和YNP处理实验时间线。RBD蛋白与弗氏佐剂乳化后皮下注射于小鼠腹部(初次免疫用完全佐剂;加强免疫用不完全佐剂)。空白(80-90周龄),未接种对照组(n=4);Vac(80-90周龄),仅接种组(n=6);Vac(80-90周龄)+YNP,接种加口服YNP处理组(120mg/kg,每2天一次,持续1周;n=6)。b,ELISA检测血清抗RBD IgG结合滴度(空白(80-90周龄)、Vac(80-90周龄),n=6;Vac(80-90周龄)+YNP,n=7,生物学重复)。P值(从左至右),*P=0.0173,*P=0.0199,P=0.0025。c,第42天测量的针对Wuhan、Beta、Delta和BA.1株的假型慢病毒中和抗体滴度(IC50)(空白(80-90周龄),n=3;Vac(80-90周龄)、Vac(80-90周龄)+YNP,n=5,生物学重复)。P值(从左至右),*P=0.0402,P=0.0007,P=0.0053,P=0.0029。d,T细胞重新分组分析的t-SNE图及相应的定量结果。e,TFH细胞中代表性基因(包括Pdc1、Cxcr5、Irf4、Bcl6、Cd40lg、IL21和Tox2)表达的点图。f,T细胞的GO富集散点图。g,B细胞重新分组分析的t-SNE图及相应的定量结果。h,B细胞中代表性基因(包括Ms4a1、Cd19、Cr2、Cd22、Ptprc、Xbp1和Sdc1)表达的点图。i,B细胞的GO富集散点图。j,免疫后第50天通过ELISpot测定再刺激脾细胞的IFNγ斑点形成细胞及统计数据(每组n=6,生物学重复)。*P=0.0119。k,CD4+ T细胞中IFNγ、IL-2和TNF的频率(每组n=4,生物学重复)。P值(从左至右),*P=0.0472,NS,P=0.0581,NS,P=0.0553。l,CD8+ T细胞中IFNγ、IL-2和TNF的频率(每组n=5,生物学重复)。P值(从左至右),P=0.0022,P=0.0004,**P=0.0015。数据表示为均值±标准误。统计分析采用双尾Student t检验。NS,不显著。
YNP通过纳米尺寸效应增强衰老树突状细胞功能
研究团队进一步探究了YNP增强树突状细胞迁移的机制。体外实验显示,由于YNP的纳米尺寸结构,即使衰老的骨髓来源树突状细胞也能有效吞噬YNP,其吞噬效率与年轻树突状细胞相当,而这种效应在微米级酵母或小分子染料中并未观察到(图5)。YNP处理能有效促进衰老树突状细胞活化,显著上调迁移标志物CCR7的表达,诱导CD4+和CD8+ T细胞产生更多IFNγ。RNA测序分析表明,YNP处理上调了衰老树突状细胞中与细胞迁移、免疫应答和趋化信号相关的基因通路。活体分布实验证实,YNP主要在小肠中积累,能有效穿过肠道黏液层与肠道树突状细胞相互作用,且肠道滞留时间显著长于普通酵母。
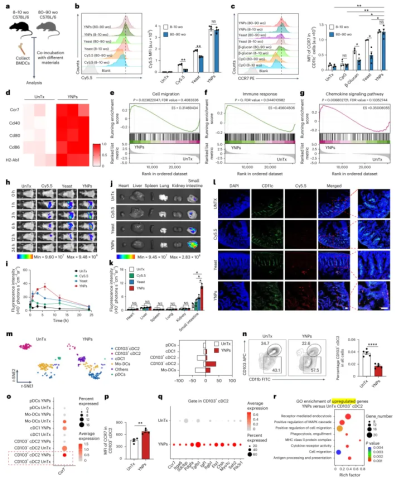
图5 | YNP增强衰老树突状细胞的迁移潜能。 a,b,年轻和老年骨髓来源树突状细胞对YNP、酵母和Cy5.5的吞噬摄取分析(每组n=4,生物学重复)。P值:(b)YNP:*P=0.0322;酵母:NS,P=0.1134;Cy5.5:NS,P=0.0709。c,流式细胞术分析不同处理后CCR7的表达(每组n=3,生物学重复)。P值:*P=0.0308,P=0.0012,*P=0.0218。d,YNP处理后老年骨髓来源树突状细胞中代表性基因的RNA测序分析(n=3,生物学重复)。e-g,GO富集分析显示YNP处理后老年骨髓来源树突状细胞中上调的通路。h,i,Cy5.5标记的酵母或YNP口服给药后不同时间点的体内生物发光成像及定量结果(每组n=3,生物学重复)。P值:(i)*P=0.0109,*P=0.0292。j,k,体外生物发光成像显示主要组织中的YNP分布及定量结果(每组n=3,生物学重复)。P值:肝脏:YNP vs UnTx P=0.1375,YNP vs Cy5.5 P=0.6258,YNP vs酵母P=0.1375;脾脏:YNP vs UnTx P=0.0629,YNP vs Cy5.5 P=0.4149,YNP vs酵母P=0.8943;肺:YNP vs UnTx P=0.0794,YNP vs Cy5.5 P=0.0522,YNP vs酵母P=0.8497;肾脏:YNP vs UnTx P=0.0591,YNP vs Cy5.5 P=0.7578,YNP vs酵母P=0.9205;小肠:YNP vs UnTx P=0.0104,YNP vs Cy5.5 P=0.0482,YNP vs酵母P=0.0489。l,小肠免疫荧光染色代表性图像。比例尺,100μm。m,树突状细胞重新分组分析的t-SNE图及相应的定量结果。n,肠道CD103-cDC2(CD103-CD11b+CD11c+MHCII+CD8-CD45+)的流式细胞术分析及相应的定量结果(每组n=5,生物学重复)。**P<0.0001。o,树突状细胞亚群中代表性基因Ccr7表达的点图。p,CCR7表达的流式细胞术分析(每组n=4,生物学重复)。**P=0.0019。q,CD103-cDC2中代表性迁移相关基因。r,CD103-cDC2中上调基因的GO富集分析。数据表示为均值±标准误。统计分析采用双尾Student t检验。NS,不显著。
YNP促进肠道树突状细胞向淋巴结迁移
为证实口服YNP诱导的迁移性cDC2确实来源于肠道,研究团队使用了光转换Kaede转基因小鼠模型。通过精确照射小肠实现肠道细胞的光转换,随后追踪这些细胞是否迁移至腹股沟淋巴结(图6)。实验结果显示,YNP处理组小鼠淋巴结中清晰检测到Kaede红色阳性细胞(即光转换后的肠道树突状细胞),数量较对照组增加了9.59倍。流式细胞术和共聚焦显微镜成像均证实了这一发现。进一步使用CD11c-DTR转基因小鼠特异性清除肠道树突状细胞后,YNP增强疫苗应答的效果被完全消除,迁移性cDC2数量、TFH细胞和浆细胞数量均显著减少,直接证明了肠道树突状细胞在YNP增强疫苗应答中的关键作用。
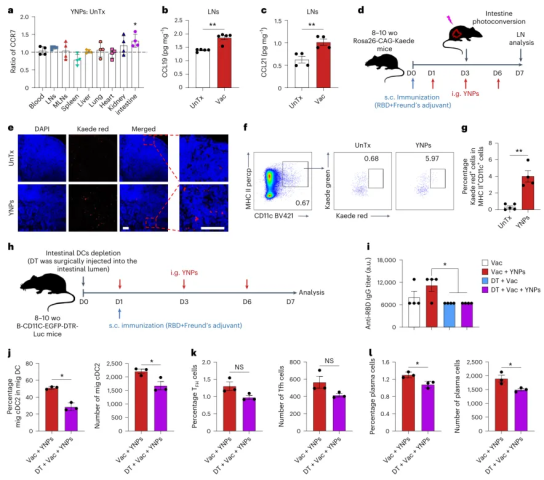
图6 | 口服YNP促进肠道树突状细胞从肠道向淋巴结迁移。 a,YNP处理小鼠各组织树突状细胞中CCR7表达的流式细胞术分析(每组n=4,生物学重复)。b,皮下免疫后腹股沟淋巴结中趋化因子CCL19的水平(每组n=5,生物学重复)。P=0.0014。c,皮下免疫后腹股沟淋巴结中趋化因子CCL21的水平(每组n=4,生物学重复)。P=0.0093。d,实验时间线:Kaede转基因小鼠用弗氏佐剂中的RBD蛋白皮下免疫。免疫后三天,对小肠树突状细胞进行光转换,第7天分析淋巴结。e,代表性共聚焦显微镜图像显示腹股沟淋巴结切片中的Kaede红色阳性细胞(光转换的肠道树突状细胞)。细胞核用DAPI复染(蓝色)。比例尺,100μm。f,g,流式细胞术定量迁移的肠道树突状细胞。Kaede红色阳性细胞设门策略(f)。淋巴结中Kaede红色阳性细胞频率的定量分析(g)(UnTx,n=5;YNP,n=4,生物学重复)。**P=0.0023。h,评估树突状细胞耗竭对YNP增强疫苗应答影响的实验方案示意图。B-CD11c-EGFP-DTR-Luc小鼠用弗氏佐剂配制的RBD蛋白皮下免疫。i,ELISA检测血清抗RBD IgG结合滴度(每组n=4,生物学重复)。*P=0.0240。j,淋巴结中迁移性cDC2(CD11b+XCR1-MHCII+CD11c+Epcam-CD45+)的比例和绝对数量(每组n=3,生物学重复)。P值(从左至右),*P=0.0114,*P=0.0373。k,l,淋巴结中TFH细胞(CD3+CD4+Foxp3-PD-1+CXCR5+)(k)和浆细胞(CD45+CD44+CD138+)(l)的比例和绝对数量(每组n=3,生物学重复)。P值(从左至右),NS,P=0.0713,NS,P=0.1031,*P=0.0181,*P=0.0387。数据表示为均值±标准误。统计分析采用双尾Student t检验。NS,不显著。
研究总结与展望
本研究系统揭示了衰老相关树突状细胞迁移缺陷是导致老年疫苗反应减弱的关键机制,并意外发现口服酵母纳米颗粒通过肠道免疫轴有效恢复老年小鼠疫苗应答。这一非侵入性策略具有安全性高、成本低、可及性强的优势,尤其是YNP主要成分β-葡聚糖的成人每日推荐摄入量至少为3克,进一步证实了其安全性潜力。研究的局限性在于目前仅使用雌性小鼠,且其他纳米材料的潜力有待探索,肠道菌群和免疫细胞的相互作用也需进一步研究。尽管如此,该发现为提升老年人群疫苗效力提供了全新的思路和方法,通过口服补充剂的方式改善免疫功能,在全球特别是在发展中国家具有广阔的应用前景。
(来源:BioMed科技)
原文出处:Kaivola J, Punovuori K, Chastney MR, Abdo H, Follain G, Mathieu M, Joshi O, Miroshnikova YA, Krautgasser F, Di Franco J, Conway JRW, Held S, Bertillot F, Hagström J, Mäkitie A, Irjala H, Ventelä S, Hamidi H, Scita G, Cerbino R, Wickström SA, Ivaska J. Restoring the tumour mechanophenotype of vocal fold cancer reverts its malignant properties. Nat Mater. 2026 Feb 20. doi: 10.1038/s41563-025-02473-7. Epub ahead of print. PMID: 41721007.
链接:https://pubmed.ncbi.nlm.nih.gov/41721007/
