公共卫生学术热点追踪
Nature:个体化mRNA疫苗,持久对抗三阴性乳腺癌,患者6年无复发
三阴性乳腺癌(TNBC),其特征为雌激素受体(ER)、孕激素受体(PR)和人表皮生长因子受体-2(HER2)均缺失,占所有浸润性乳腺癌的 15% 至 20%,且相较于其他乳腺癌亚型,其早期复发的风险更高,是乳腺癌中最凶险的亚型。
三阴性乳腺癌(TNBC)即使在早期阶段也容易复发和转移,复发率在诊断后大约三年达到峰值,此后迅速下降。DNA 修复缺陷、内在基因组不稳定性和免疫原性肿瘤微环境使得 TNBC 成为利用体细胞癌症突变(可作为新抗原)进行个体化疫苗接种的有力候选对象。
近日,BioNTech 公司的研究人员在国际顶尖学术期刊 Nature 上发表了题为:Individualized mRNA vaccines evoke durable T cell immunity in adjuvant TNBC 的研究论文。
该研究揭示了个体化 mRNA 疫苗在三阴性乳腺癌(TNBC)中诱导了持久的 T 细胞免疫反应,14 例患者中有 11 例接种 mRNA 疫苗后在长达六年内保持无复发状态。

三阴性乳腺癌(TNBC)常伴随转移性复发,即使在早期阶段也是如此。
在这项研究中,研究团队对 14 例接受了手术及新辅助治疗或辅助治疗后的三阴性乳腺癌(TNBC)患者评估了个体化新抗原 mRNA 疫苗的效果。
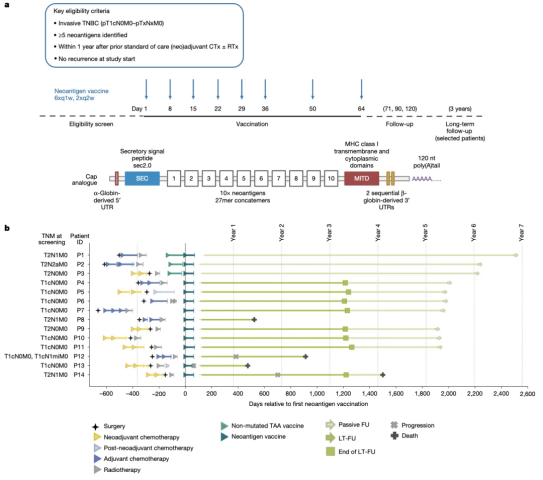
结果显示,在几乎所有患者的外周血中,均检测到 mRNA 疫苗诱导的、靶向多个新抗原的高强度 T 细胞应答(多数为新生应答),且这些 T 细胞应答在数年内保持功能活性。对个体患者的表征分析显示,这些 T 细胞大部分分化为两个亚群:一类是具有“即用型”细胞毒性效应 T 细胞标志的晚期分化表型,另一类是具有干细胞样记忆表型的 T 细胞。
全部 14 例患者中,有 11 例患者接种 mRNA 疫苗后在长达六年内保持无复发状态。仅 3 例患者出现复发:疫苗诱导 T 细胞应答最弱的个体复发,但后续的抗 PD-1 治疗使其获得了完全缓解;另一例患者肿瘤主要组织相容性复合体(MHC)I 类表达低下,疫苗接种期间出现 MHC-I 类缺陷细胞扩增;第三例为 BRCA 阳性患者,其复发实际上源于遗传学差异的原发肿瘤。
总的来说,这项研究证实了个体化 RNA 疫苗在三阴性乳腺癌(TNBC)领域的可行性,该研究记录了疫苗诱导的功能性新抗原特异性 T 细胞的持久存在,并为可能的免疫逃逸机制提供见解,将为未来研究提供指导。
(来源:生物世界)
原文出处:Sahin U, Schmidt M, Derhovanessian E, Cortini A, Vogler I, Omokoko T, Godehardt E, Attig S, Newrzela S, Grützner J, Bidmon N, Bolte S, Brachtendorf S, Stuhlmann T, Langer D, Brüne D, Blake J, Feldner A, Lindman H, Schneeweiss A, Eichbaum M, Türeci Ö. Individualized mRNA vaccines evoke durable T cell immunity in adjuvant TNBC. Nature. 2026 Feb 18. doi: 10.1038/s41586-025-10004-2. Epub ahead of print. PMID: 41708868.
链接:https://pubmed.ncbi.nlm.nih.gov/41708868/
