公共卫生学术热点追踪
PNAS | 清华大学丁强等团队发现戊肝病毒复制必需的两个关键宿主蛋白,为开发首个抗HEV特效药奠定基础
戊型肝炎病毒(HEV)是全球范围内急性病毒性肝炎的主要致病因素,每年约导致2000万例感染。尽管中国已有疫苗可用,但目前尚无获批的直接抗病毒药物,且HEV复制所需的宿主因子仍不明确。
2026年3月4日,清华大学丁强,北京大学王麟和俄亥俄州克利夫兰诊所研究部Xianfang Wu共同通讯在PNAS 在线发表题为“EIF4H and YBX1 are essential host factors for hepatitis E virus replication and pathogenesis”的研究论文。该研究通过在全基因组范围内利用复制子系统进行CRISPR/Cas9敲除筛选,鉴定出真核翻译起始因子4H(EIF4H)和Y盒结合蛋白1(YBX1)是HEV复制与致病的关键宿主因子。敲除任一因子均显著抑制了HEV基因型1、3和4的复制,以及在肝癌细胞和人诱导多能干细胞来源的肝细胞样细胞中的HEV感染与病毒产生,而对SARS-CoV-2、乙型肝炎病毒、丙型肝炎病毒和寨卡病毒无影响,这凸显了二者在HEV感染中的特异性作用。
机制上,EIF4H通过其甲基转移酶-Y-木瓜蛋白酶样蛋白酶区域与ORF1相互作用,且EIF4H缺失会改变ORF1相关复制复合物的组成。相比之下,YBX1对ORF1的翻译和RNA结合并非必需,但特异性参与ORF1的蛋白水解加工,这是组装功能性复制机器的先决条件。EIF4H敲除大鼠和肝脏特异性YBX1敲除大鼠对大鼠HEV-C1感染表现出高度抵抗力,其病毒排出显著减少,肝脏和肠道病毒载量受到抑制,并免受肝脏病理损伤。综上所述,本研究确立了EIF4H和YBX1作为HEV感染与致病的关键宿主因子,并揭示了潜在的抗病毒干预靶点。

戊型肝炎病毒(HEV)感染是一项重大的公共卫生问题,全球每年估计发生2000万例感染。HEV感染通常具有自限性,但在免疫功能受损的患者中可转为慢性,例如移植受者和人类免疫缺陷病毒(HIV)感染者。在孕妇中,HEV感染与严重的临床结局相关,孕晚期死亡率可高达30%。尽管存在这些严重的健康影响,目前尚无获批用于HEV治疗的直接抗病毒药物,仅有一种疫苗在中国获准使用,这凸显了对新治疗策略的迫切需求。
HEV属于戊型肝炎病毒科(Hepeviridae)和帕斯拉戊型肝炎病毒属(Paslahepevirus)。在该属内,HEV基因型表现出不同的生物学和流行病学特征。基因1型和2型仅感染人类,是导致大规模水源性暴发的主要原因;而基因3型和4型为人畜共患,以猪和鹿为主要宿主,引起散发性及食源性感染。HEV基因组为一条长约7.2 kb的正链单股RNA,编码三个开放阅读框(ORF):ORF1、ORF2和ORF3,其中在基因1型中还发现了一个额外的ORF4。ORF1编码一个大的非结构多蛋白,包含多个保守结构域:甲基转移酶、Y结构域、一个常被称为木瓜蛋白酶样半胱氨酸蛋白酶(PCP)的区域、高变区(HVR)、解旋酶(Hel)以及RNA依赖性RNA聚合酶(RdRp),这些结构域对于病毒RNA复制和亚基因组RNA转录至关重要。
ORF1被认为是构成病毒复制酶的核心。然而,ORF1是作为一个完整的前体发挥作用,还是经过蛋白水解加工产生功能性亚基,这一直是一个长期悬而未决的问题。解决此问题的进展受到感染期间ORF1丰度低以及缺乏高质量抗体的限制,这使其检测和表征变得复杂。早期使用异源表达或体外翻译实验的研究关于ORF1加工得出了相互矛盾的结论,一些研究报道了PCP介导的自剪切,而另一些则未检测到切割。另有报告提出,宿主蛋白酶如凝血酶或因子Xa,可能参与在特定位点切割ORF1。更具说服力的证据来自具有复制能力的系统,这些系统揭示了与复制工厂组装同时出现的、更小的ORF1衍生产物。最近,一项独立研究证明了ORF1存在蛋白酶体依赖性加工,产生一种被称为HEV来源的SMAD激活因子的截短产物,该产物可激活促纤维化的TGF-β信号通路,从而促进纤维化。尽管其精确机制仍有争议,但来自具有复制能力系统的累积证据支持ORF1存在受调控的加工过程。
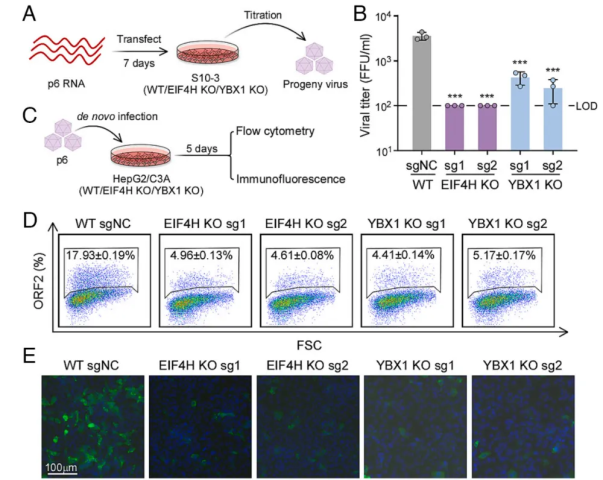
先前的研究已强调了参与HEV生命周期不同阶段的几种宿主因子。据报道,硫酸乙酰肝素蛋白聚糖(HSPGs)、ras相关蛋白Rab5/Rab7、表皮生长因子受体(EGFR)、组织蛋白酶L(CTSL)和整合素β1(ITGB1)可促进病毒的摄取和运输。HSP90已被证明在病毒复制中发挥重要作用,而膜联蛋白A2(ANXA2)和肿瘤易感基因101(TSG101)对于病毒颗粒的有效释放至关重要。然而,HEV复制的潜在机制仍不明确,部分原因是传统HEV培养系统存在局限性。虽然蛋白质组学研究揭示了与ORF1存在交互作用的宿主蛋白,表明其在调节HEV复制中的作用,但许多对病毒复制至关重要的宿主因子仍属未知。最近,一项全基因组CRISPR/Cas9筛选鉴定出Rab5A是HEV复制所必需的宿主因子。
为了进一步剖析HEV与宿主的交互作用,已开发了多种实验模型。人类肝癌细胞系,如Huh7和HepG2/C3A,因其对HEV感染的易感性而被广泛使用。人类诱导多能干细胞来源的肝细胞样细胞(HLCs)提供了一个更具生理相关性的系统,能够支持高效的HEV复制。此外,动物模型使得能够在体内分析病毒复制和致病机制。兔对某些HEV毒株天然易感,已被用于研究人畜共患传播和致病机制。感染大鼠HEV毒株(如属于Rocahepevirus属的HEV-C1)的大鼠是研究HEV的有用小动物模型,因为尽管存在遗传差异,大鼠HEV-C1与人类HEV具有相似的基因组组织和复制策略。实验性感染人类HEV的长爪沙鼠和猴子进一步揭示了感染动态和致病机制。然而,这些动物模型有限的遗传可操作性限制了它们在病毒-宿主交互作用详细机制研究中的应用。
病毒复制子系统保留了复制能力但缺乏病毒颗粒组装所需的基因,是研究病毒复制和病毒-宿主交互作用的有力工具,特别是对于像HEV这样难以在体外增殖的病毒。通过在HEV复制子中进行全基因组CRISPR/Cas9敲除筛选,作者鉴定出真核翻译起始因子4H(EIF4H)和Y盒结合蛋白1(YBX1)是HEV复制和致病所必需的宿主因子。综上所述,作者的研究为理解HEV复制的分子机制提供了见解,这可能有助于开发有效的治疗靶点。
(来源:iNature)
原文出处:Ju X, Dong L, Liu T, Zhang F, Sun X, Schwoerer MP, Ren W, Gong M, Ploss A, Qin W, Wu X, Wang L, Ding Q. EIF4H and YBX1 are essential host factors for hepatitis E virus replication and pathogenesis. Proc Natl Acad Sci U S A. 2026 Mar 10;123(10):e2529289123. doi: 10.1073/pnas.2529289123. Epub 2026 Mar 4. PMID: 41779781.
链接:https://pubmed.ncbi.nlm.nih.gov/41779781/
